摘要:近期发现28批次药品不符合规定,引发社会关注。这些药品存在质量问题,可能对患者健康造成潜在威胁。深度解析显示,问题涉及生产流程、原料采购、监管环节等方面。此事警示药品生产企业和监管部门需加强合作,提高药品质量监管力度,确保公众用药安全。应反思当前药品监管体系是否健全,采取有效措施预防类似问题再次发生。
本文目录导读:
关于药品质量的问题再次引起社会广泛关注,涉及药品安全的问题不容忽视,据最新数据显示,有28批次药品不符合规定,这一事件再次敲响了药品安全问题的警钟,本文将围绕这一事件展开分析,探讨药品不符合规定的原因、影响以及应对措施。
事件概述
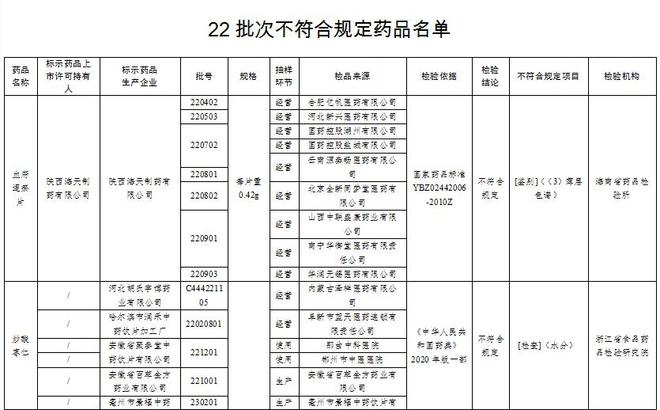
国家药品监管部门发布通告,经过抽检发现,有28批次药品存在质量问题,不符合规定,这些药品涉及多个品种,包括抗生素、感冒药、降压药等常用药物,这一事件引起了社会的广泛关注,引发了公众对药品安全的担忧。
不符合规定药品的原因分析
1、药品生产环节的问题:部分药品生产企业在生产过程中存在管理不严、操作不规范等问题,导致药品质量不达标。
2、药品监管力度不足:药品监管部门在监管过程中存在盲区,监管力度不足,导致部分不合格药品流入市场。
3、市场竞争压力:部分药品生产企业为了降低成本,追求利润最大化,采用劣质原料或简化生产工艺,导致药品质量下降。
不符合规定药品的影响
1、公众健康威胁:不符合规定的药品可能无法有效治疗疾病,甚至可能加重病情,对公众健康造成威胁。
2、社会信任度下降:药品安全事件频发会导致公众对药品行业的信任度下降,影响社会的稳定。
3、医药行业发展受阻:药品安全问题会影响医药行业的声誉,阻碍行业的健康发展。
应对措施
1、加强药品生产环节的监管:药品监管部门应加强对药品生产企业的监管力度,确保生产企业严格按照规定生产药品。
2、加大抽检力度:药品监管部门应加大对药品的抽检力度,提高抽检频率和覆盖面,及时发现并处理不合格药品。
3、强化企业责任:药品生产企业应自觉履行社会责任,加强质量管理,确保药品质量。
4、完善法律法规:政府应完善药品管理相关法律法规,加大对违法行为的处罚力度,提高违法成本。
5、加强公众教育:提高公众对药品安全的认识,引导公众安全用药,合理购药。
深入反思与未来展望
1、反思现行药品管理制度:针对此次事件,我们需要深入反思现行的药品管理制度,查找制度漏洞,完善管理制度。
2、建立长效机制:建立药品安全长效机制,确保药品监管工作的持续性和稳定性。
3、加强国际合作:借鉴国际先进经验,加强国际合作,提高我国药品监管水平。
4、科技创新助力药品质量提升:鼓励医药企业加大科研投入,通过科技创新提高药品质量。
5、未来展望:我们相信,在政府、企业和社会各界的共同努力下,我国药品安全问题一定能够得到妥善解决,确保公众用药安全。
涉及28批次药品不符合规定的事件再次敲响了药品安全问题的警钟,我们必须加强药品生产环节的监管、加大抽检力度、强化企业责任、完善法律法规、加强公众教育等措施,确保药品质量,保障公众健康,我们需要深入反思现行药品管理制度,建立长效机制,加强国际合作,通过科技创新助力药品质量提升,让我们共同努力,为创造一个安全、健康的医药环境而奋斗。


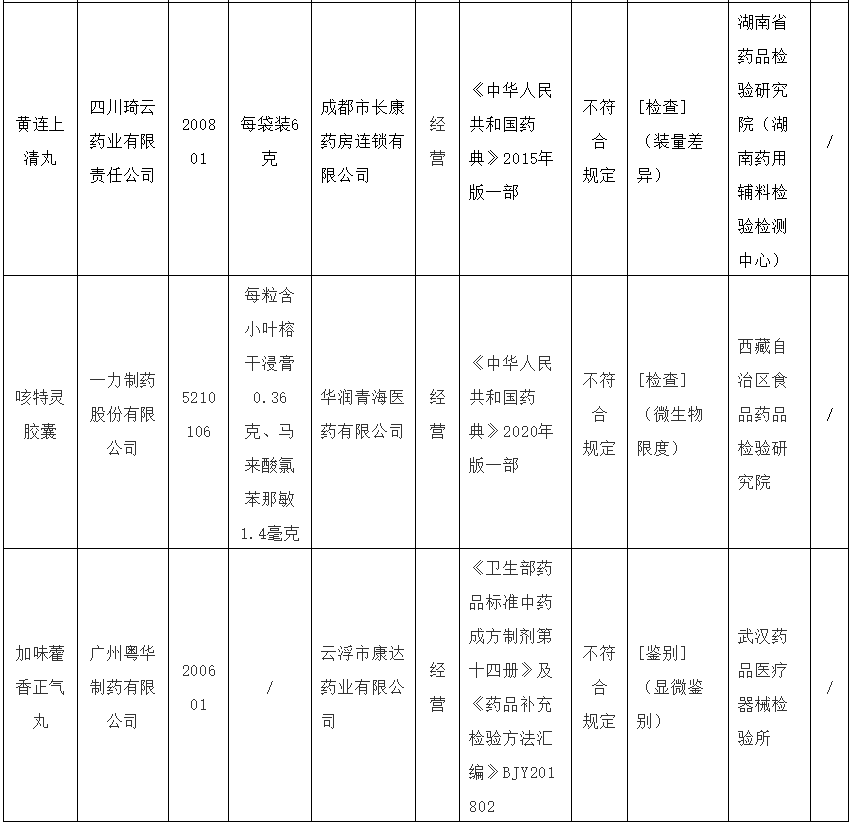
 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号